健康问题


慢病管理

健康动态

知识互动

数据统计




健康问题


慢病管理

健康动态

知识互动

数据统计




细胞是生物体基本的结构和功能单位,细胞储存通过一定的方法将细胞中的APSC多能细胞保存一定的期限,保证细胞的功能和活性不受明显的影响。主要包括免疫细胞储藏和干细胞储藏,而其中免疫细胞跟人体健康息息相关,是治疗很多疾病的有效武器,因此,在身体健康的时候储藏一定量的免疫细胞,相当于为将来的健康买了一份特殊的保险。
随着年龄的增加,免疫系统衰退引起的免疫功能下降,容易引起各种疾病。为了有效预防疾病,预先将当下健康年轻态的免疫细胞,通过安全采集并超低温冻存起来,在有抗衰防病之需时,再回输体内,来对抗疾病、延缓衰老、增强抵抗力。 将自体细胞进行存储并在未来用于可能的疾病治疗,这是在再生医疗技术不断突破的前提下一种有效生命资源存储。
免疫细胞是健康的守护者,现代人压力大、饮食不正常、常熬夜,导致免疫系统较为虚弱,容易引起癌症等各种疾病。最重要的是,随着年龄渐长,细胞老化使得免疫力逐渐下降。 人体免疫系统的免疫力在20岁达到高峰,到了40岁时,就只剩20岁的一半,到了70岁,又只有20岁时的1/10,所以趁着现在,提早存储健康的免疫细胞,因为今天永远比明天更年轻!
1)免疫细胞的数量、质量与生命息息相关,它会随着年龄增长逐渐减少,趁现在去储存自己最健康的免疫细胞,在未来可补充自身免疫细胞数量; 2)空气、水、食物等的污染正时刻危及健康,工作、生活等压力正让人处于亚健康状态,急需应用细胞进行免疫调节; 3)免疫细胞治疗已成为手术、放疗、化疗之后又一治疗癌症的手段,可配合传统治疗达到更好的效果,储存免疫细胞就是储存了生命的种子; 4)人口老龄化严重,储存、使用免疫细胞可延缓衰老,提高生活质量。
1)治疗恶性肿瘤 当不幸罹患癌症时,把储存的免疫细胞进行复苏、激活和扩增,输回体内,可以清除体内的癌细胞,控制癌症的发展,达到延长生存期和改善生活质量等多重目标; 2)抗衰老 衰老是人体机能变缓的直接表现,也是一种自然的过程,免疫细胞可延缓衰老进程; 3)调节亚健康 亚健康是人体介于健康和疾病的临界点,也是身体发出的警讯,如果不重视,可能发生不可逆转的健康危机,免疫细胞可明显调节亚健康; 4)提高免疫力 实验证实,定期回输免疫细胞,可显著提升人体免疫力,预防疾病,预防癌症的发生。
临床证实利用患者的免疫细胞治疗是有一定程度的疗效,但此时人体的免疫细胞是虚弱的,有缺陷的,这样的免疫细胞无法发挥健康时的效益,会降低免疫细胞治疗的成效,这也就是为什么要在健康的时候,将免疫细胞存起来的原因。
储存免疫细胞虽无年龄限制,然而就免疫细胞发展与健全的条件,建议最好年满18岁,免疫系统发育健全之后再来进行更好,但20岁是免疫系统的最高峰。新生儿降生之时,将其脐带、脐带血和胎盘保存到细胞库,一根新生儿脐带分离出来的间充质干细胞可供上万人治疗使用。
当然可以,因为今天永远比明天更年轻,年轻的时候,及早储存,等于买了更健康的保障。
在身体健康状况最好的时候来储存免疫细胞,当然是最好。但身体好不好,并非看外表,而是要经过精密的检查才能断定。在免疫细胞采集存储前,会先进行体检。
免疫细胞泛指参与免疫反应的细胞,可特别识别抗原,产生特异性免疫反应的淋巴细胞。 目前的免疫细胞治疗技术,主要应用在癌症肿瘤、病毒感染等方面,癌症肿瘤包括淋巴癌、乳癌、子宫颈癌、肝癌等,在临床上有许多成功的案例。而治疗的效率及成果,有没有好的免疫细胞是关键因素之一。若免疫细胞不好,治疗效果会打折扣,当人们患重大疾病(如肿瘤)时,利用储存的免疫细胞,结合先进的CAR-T细胞免疫治疗技术,可有效杀灭癌细胞。其疗效优于利用发病时免疫细胞治疗的效果。目前,细胞免疫治疗技术是最具希望治愈肿瘤的方法。
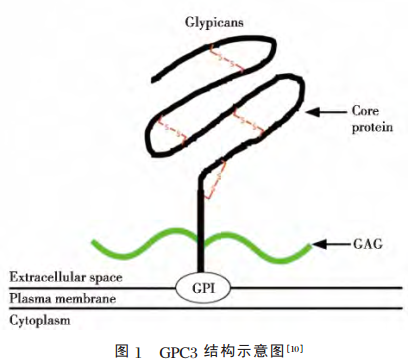
磷脂酰肌醇蛋白聚糖3(glypican 3,GPC3)在调控细胞生长和分化方面起重要作用,与肝癌的发生、发展密切相关。GPC3在肝癌组织中特异性高表达,从而提示GPC3对肝癌诊断具有明显的灵敏性和特异性,可作为肝癌治疗的新靶点。该文综述GPC3的结构功能及基于GPC3靶点的肝癌免疫治疗进展,并讨论其作为未来肝癌治疗靶点的前景。 本公司开发了针对GPC3的肝癌治疗性CAR-T细胞,能够很好的对GPC3阳性的肝癌细胞进行杀伤,有效的缓解患者的病情。
肝癌即肝脏恶性肿瘤,可分为原发性和继发性两大类。原发性肝脏恶性肿瘤起源于肝脏的上皮或间叶组织,前者称为原发性肝癌,是我国高发的,危害极大的恶性肿瘤;后者称为肉瘤,与原发性肝癌相比较较为少见。继发性或称转移性肝癌系指全身多个器官起源的恶性肿瘤侵犯至肝脏。一般多见于胃、胆道、胰腺、结直肠、卵巢、子宫、肺、乳腺等器官恶性肿瘤的肝转移。、 本公司开发了针对GPC3的肝癌治疗性CAR-T细胞,能够很好的对GPC3阳性的肝癌细胞进行杀伤,有效的缓解患者的病情。

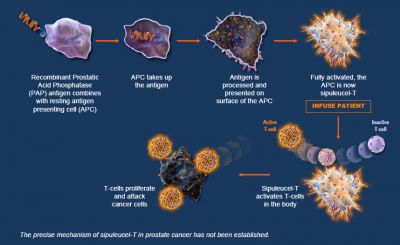
肿瘤疫苗(tumor vaccine)是近年研究的热点之一,其原理将肿瘤抗原以多种形式如:肿瘤细胞、肿瘤相关蛋白或多肽、表达肿瘤抗原的基因等,导入患者体内,克服肿瘤引起的免疫抑制状态,增强免疫原性,激活患者自身的免疫系统,诱导机体细胞免疫和体液免疫应答,从而达到控制或清除肿瘤的目的。
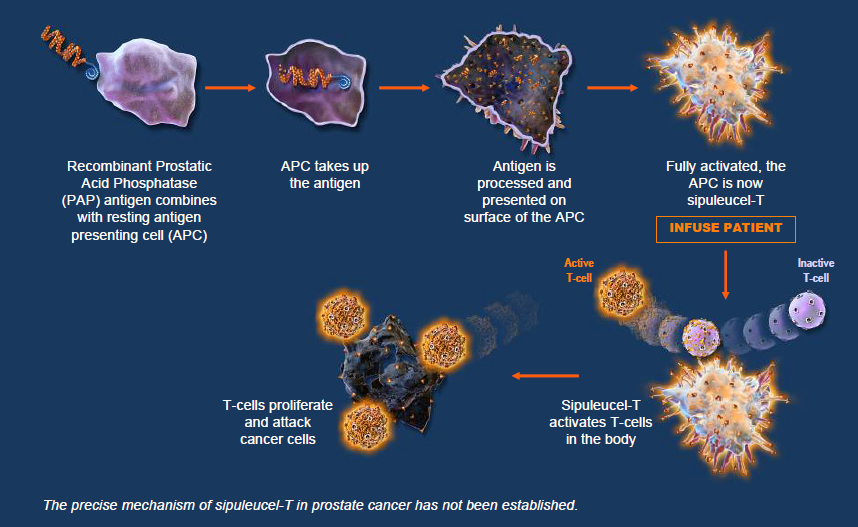
2010年4月,美国食品药品监督管理局(FDA)批准Provenge/ sipuleucel-T用于治疗晚期前列腺癌,使其成为第一个自体主动免疫疗法药及第一个真正的治疗性癌症疫苗,为其他同类产品的研发铺平道路。
癌症的传统治疗手段如:手术治疗、放射治疗和药物治疗等,均具有一定的局限性。由于靶向性较差,放射治疗和药物治疗易损伤正常细胞,产生不良反应。恶性肿瘤具有易侵袭和易复发的生物学特征,因此需要靶向性更好、毒性更小的治疗方案。随着肿瘤基因组学的发展,生物免疫疗法成为肿瘤治疗的第四种手段。有研究证明,肿瘤细胞具有肿瘤抗原,免疫系统能通过识别肿瘤抗原区别肿瘤细胞和正常细胞。肿瘤疫苗通过表达特异性的、具有免疫原性的肿瘤抗原(如:多肽、DNA和RNA等),在细胞因子、趋化因子等佐剂的辅助下,激活或加强机体自身抗肿瘤免疫,进而杀伤和清除肿瘤细胞。目前,肿瘤疫苗已成为肿瘤治疗领域的研究热点 。
目前,已上市和正在开发中的肿瘤疫苗大致可分为4类,分别是:全细胞疫苗、肿瘤多肽疫苗、基因工程疫苗和抗体肿瘤疫苗。
全细胞疫苗根据细胞来源又可分为肿瘤细胞疫苗和树突状细胞(DC)疫苗。在肿瘤特异性抗原尚未明确的情况下,肿瘤全细胞疫苗有其独特的优势。肿瘤全细胞疫苗包含了全系列的肿瘤相关抗原(TAA),富含CD8T细胞CD4辅助T细胞的抗原表位,能同时表达MHCⅠ和Ⅱ类限制抗原,引起全面有效的抗肿瘤应答、诱导形成长效记忆T细胞。 肿瘤全细胞疫苗的传统制备方法是采用物理、化学或生物方法(紫外线照射、加热和神经氨酸酶等)处理选取自体或同种异体肿瘤细胞,该疫苗保留了免疫原性但无致瘤性。随着现代生物技术的发展,目前已能实现目的基因片段在肿瘤细胞的导入,如:MHC-1分子、共刺激细胞因子(IL-2、IL-12和GM-CSF)等,免疫原性进一步提高。 DC作为功能最强的专职APC,是引发肿瘤抗原强免疫应答的关键。但肿瘤宿主体内肿瘤DC浸润较少且功能受损,因此将载有肿瘤抗原的宿主DC进行体外培育,制备DC肿瘤疫苗,是获得肿瘤宿主强免疫应答的有效策略。2010年4月,美国FDA批准了首个以DC为主要效应细胞的自体细胞免疫治疗药物sipuleucel-T (Provenge),其适应症为无症状或轻微症状的转移性去势抵抗性前列腺癌治疗。
采用肿瘤细胞表面洗脱的抗原多肽或肿瘤细胞内部异常表达的蛋白制备多肽疫苗,具有特异性强、安全性高的优点。进一步对氨基酸残基修饰、氨基酸序列改变或者制备热休克蛋白-肽复合物,不仅可有效提高多肽抗原的特异性,而且避免与宿主细胞相似导致自身免疫。随着大量肿瘤抗原和多肽表位的发现,以及相应免疫方案的提出和实施,多种肿瘤多肽疫苗逐渐进入临床研究。如韩国公司KAEL-Gem Vax开发的胰腺癌疫苗GV1001、葛兰素史克公司(GSK)开发的二价宫颈癌疫苗Cervarix等。此外,近5年出现了一些新一代肿瘤多肽疫苗,其中,长多肽疫苗不同于仅包含一种或几种抗原表位的经典多肽疫苗,多价长多肽疫苗包含几种人白细胞抗原(HLA)类型限制性分子,能同时引起CTL和T辅助细胞效应。
利用基因工程技术将编码肿瘤特异性抗原的基因负载到重组病毒载体或质粒DNA上,直接注入人体。借助载体本身或者人体基因表达系统,能持续引起特异性的体液免疫和细胞免疫,这是基因工程疫苗较其他肿瘤疫苗无法比拟的优势,因而成为肿瘤生物治疗研究的热点。研究证明,将编码细胞因子、细菌蛋白的DNA与基因工程疫苗的质粒DNA融合,可以有效提高其免疫原性,引起强免疫应答。
根据依赖抗体细胞介导的细胞毒性作用(ADCC)理论设计的单克隆抗体肿瘤疫苗,是疫苗发展的一个新方向。单抗与相应的抗原能高度特异性结合,具有较好的分子靶向功能。目前,单克隆抗肿瘤药物有两类:一是抗肿瘤的单抗;二是抗肿瘤单抗耦联物,或称免疫偶联物。单克隆抗体药物与肿瘤抗原结合,共同刺激DC,激发CD8T细胞作用,这项技术在黑色素瘤和乳腺癌治疗上获得显著进展。FDA于2011年3月批准百时美施贵宝的YERVOY单药疗法,用于不能手术切除或转移性黑色素瘤患者的治疗 。此外,抗肿瘤单抗曲妥珠单抗(Herceptin)对于人HER-2阳性的转移性乳腺癌有较好的治疗作用 。
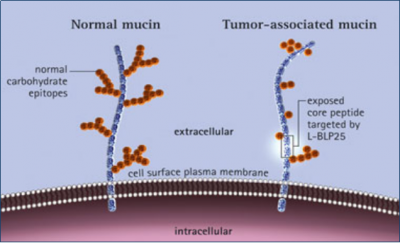
粘蛋白1(MUC1)是muc1基因编码的高分子量、高糖基化的跨膜蛋白,MUC1正常情况下主要表达于许多分泌性器官的细胞膜顶端,呈顶端表达,极性分布,对正常的上皮起润滑和保护作用,同时还介导信号转导,研究发现MUC1在许多实体瘤中异常表达,并与肿瘤的发生、发展和转移密切相关。 研究发现99%的肿瘤患者MUC1均异常表达,主要体现在表达量增加,糖基化异常,其中糖基化异常为肺癌治疗性CAR-T提供了良好的靶点。
具有糖基化特质的靶点抗原就成为了颇具吸引力的CAR-T目标。蛋白糖基化是肿瘤细胞恶性转化中的一个重要因素,还具有调节免疫耐受的作用。蛋白糖基化的启动是从聚糖共价联接到天冬酰胺残基(N-连接)、或者联接到丝氨酸或苏氨酸残基(O-连接)而开始的。其中,O连接的糖基化,是N-乙酰半乳糖胺(GalNac)在大约20种人多肽半乳糖胺转移酶(半乳糖胺-TS)催化下,联接到丝氨酸或苏氨酸残基而形成的。在正常细胞中,附着于蛋白质骨架的GalNAc残基在T合酶的作用下,进一步延伸,形成核心1结构(半乳糖-GalNAc-a-丝氨酸/苏氨酸)。在肿瘤细胞表面,最常见的异常糖基化形式是Tn(GalNAca1-O-Ser/Thr)和sialy-Tn(唾液酸-Tn,STn)(NeuAca2-6-GalNAca1-O-Ser/Thr)。而Tn的富集主要是由于正常细胞的糖链合成时所必须的伴侣蛋白Cosmc在肿瘤细胞发生突变、或者表观遗传学导致的基因沉默,最终影响了T合成酶活性丧失的缘故。Tn和STn异常糖基化形式在肿瘤细胞表面的MUC1蛋白上非常常见。但在健康个体上,不会有Tn抗原的表达,而且人体有天然的抗Tn的IgM抗体。 由Avery Posey博士和Carl June博士领导的研究小组,用Tn-抗原特异性的单抗5E5进行CAR-T的构建,对Cosmc突变的具有Tn抗原表位的Jurket细胞株、以及MUC1+的胰腺癌细胞株进行体内外试验,发现抗Tn-MUC1-CAR-T细胞可以高效、特异杀伤肿瘤细胞。